استئصال الغدة الدرقية في ايران | افضل دكتور جراح وتكلفة
أفضل مستشفى
نقدم أفضل مستشفى لعلاجات السرطان
أفضل الأطباء
نقدم أفضل الأطباء لعلاج السرطان
افضل سعر
نحاول تقديم أفضل الخدمات بالسعر العادي
استئصال الغدة الدرقية في ايران | افضل دكتور جراح وتكلفة
• تكاليف منخفضة
• البورد الجراحين المرخصين
• جودة الرعاية الصحية
• وقت انتظار أقل
• مستشفى معتمد
• الخدمة الشخصية
• القدرة اللغوية
• سهولة التأشيرة الطبية
• العلاج بالتقنية المتقدمة
• حضور قوي في مجال الرعاية الصحية المتقدمة ، على سبيل المثال الزرع - نسبة نجاح عالية في العملية
عيادات نشطة للمرضى الدوليين:
عيادة الشهيد دستاني ، عيادة أمراض الدم والأورام وزراعة الخلايا الجذعية ، عيادة الطب النووي والعيادة الخاصة.
العيادات: المسالك البولية ، أمراض الكلى ، الرئة ، الجراحة العامة ، الغدد الصماء ، أمراض الجهاز الهضمي ، أمراض النساء ، القبالة ، الفترة المحيطة بالولادة ، العقم ، جراحة الوجه والفكين ، علم الوراثة ، الأمراض الجلدية ، جراحة العظام ، جراحة الأعصاب ، القلب ، جراحة القلب ، جراحة الأوعية الدموية ، طب الأعصاب ، الروماتيزم ، الأذن والأنف. طب الأسنان ، الأمراض المعدية ، علاج النطق ، الألم ، التغذية والعلاج الغذائي ، التخدير ، الداء البطني ، تليف الكبد ، بهجت ، العيون ، الطب النفسي ، صحة الرجال
الأقسام السريرية: المختبر السريري ، علم الأمراض ، التصوير والصيدلة
العيادات: EMG-EEG ، تنظير القصبات ، قياس التنفس ، قياس كثافة العظام ، الطب النووي ، غسيل الكلى ، العلاج الطبيعي ، التنظير ، تخطيط صدى القلب ، اختبار التمرين ، السيطرة على الألم ، إعادة التأهيل والطب الرياضي.
استئصال الغدة الدرقية في ايران | افضل دكتور جراح وتكلفة
استئصال الغدة الدرقية هو عملية جراحية لإزالة الغدة الدرقية بالكامل أو جزء منها. يشار إليه في أمراض الغدة الدرقية المختلفة: سرطان الغدة الدرقية ، عقيدات سرطانية أو كبيرة الحجم ، تضخم الغدة الدرقية الضاغط ، إلخ.
استئصال الغدة الدرقية في ايران | افضل دكتور جراح وتكلفة
استئصال الغدة الدرقية في ايران
ما هو استئصال الغدة الدرقية؟
استئصال الغدة الدرقية في ايران
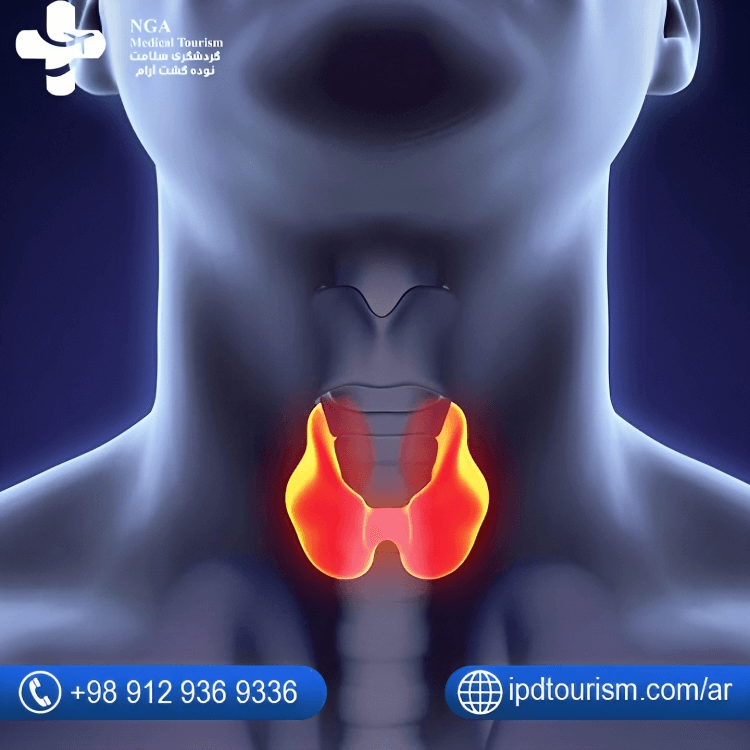
يشمل استئصال الغدة الدرقية الإزالة الجزئية أو الكلية للغدة الدرقية.
تتكون الغدة من كرتين (ومن هنا شكل الفراشة) تقعان في قاعدة العنق ، تحت تفاحة آدم ، تنظم الغدة الدرقية معدل التمثيل الغذائي للعديد من الأعضاء ، عبر هرمونات T3 و T4 التي تفرزها. لذلك فهي تلعب دورًا مهمًا جدًا في أجسامنا.
كيف يتم إجراء استئصال الغدة الدرقية؟
تتم العملية تحت تأثير التخدير العام. تستمر من 40 دقيقة إلى 1h30. يوضع المريض على ظهره ، ويمتد رأسه قليلاً.
يقوم الجراح بعمل شق أفقي بطول بضعة سنتيمترات في قاعدة العنق. ثم يشرع في استئصال الغدة الدرقية ، جزئيًا أو كليًا ، اعتمادًا على دلالة التدخل.
في حالة استئصال العقدة البسيط ، يتم إجراء فحص مجهري يسمى “الفحص الخارجي” أثناء التدخل من أجل التحقق من الطبيعة الدقيقة للعقدة التي تمت إزالتها. اعتمادًا على النتيجة ، قد يُطلب من الجراح إجراء عملية استئصال أكثر شمولاً مما كان مخططًا له في البداية.
في نهاية العملية ، يتم ترك مصفاة صغيرة في مكانها ، ثم يتم إغلاق الشق عادةً باستخدام دبابيس ، مما يعطي أفضل النتائج الجمالية.
متى يتم إجراء استئصال الغدة الدرقية؟
يشار إلى استئصال الغدة الدرقية في أمراض الغدة الدرقية المختلفة:
في حالة وجود عقيدة درقية مشكوك فيها أو سرطانية: عقيدة الغدة الدرقية عبارة عن تورم يتطور في أنسجة الغدة الدرقية. في كثير من الأحيان ، خاصة عند النساء فوق سن الخمسين ، غالبًا ما تكون حميدة. ومع ذلك ، في 5 ٪ من الحالات ، هو سرطاني. في بعض علامات التحذير (عوامل الخطر ، الحجم وخصائص الموجات فوق الصوتية للعقيدة ، مستوى TSH) ، سيتم إجراء الوخز الخلوي للتحقق من طبيعة العقدة. إذا كانت النتيجة مطمئنة ، فإن المراقبة البسيطة للعقدة عن طريق الموجات فوق الصوتية كافية. إذا أظهرت النتائج وجود شخصية مشكوك فيها ، يشار إلى استئصال شحمة الغدة الدرقية ؛
في وجود عقيدة حميدة يسبب حجمها الكبير (قطرها أكثر من 25 مم) صعوبة في البلع و / أو التنفس و / أو التحدث ؛
في حالة تضخم الغدة الدرقية الانضغاطي (زيادة حجم الغدة الدرقية) مما يسبب صعوبة في البلع والتنفس ؛
في حالة سرطان الغدة الدرقية.
في حالة تضخم الغدة الدرقية متعدد العقيدات: تتطور العقيدات المتعددة في فصين من الغدة الدرقية ، ويزداد حجمها داخل الغدة الدرقية نفسها (تضخم الغدة الدرقية). قد يكون استئصال الغدة الدرقية ضروريًا إذا كانت العقيدات كبيرة ، أو إذا كانت تمثل طابعًا مشبوهًا للوخز الخلوي أو إذا تسبب تضخم الغدة الدرقية في الضغط ؛في حالات معينة تسمى عقيدات الغدة الدرقية “الساخنة” أو “السامة” ، أي إفراز كمية كبيرة من هرمونات الغدة الدرقية وبالتالي تسبب فرط نشاط الغدة الدرقية ؛
في حالة مرض جريفز ، أمراض المناعة الذاتية التي تسبب فرط نشاط الغدة الدرقية. في حالة الانتكاس بعد العلاج الدوائي الأول ، يُقترح الجراحة أحيانًا.
اعتمادًا على الدلالة ، سيكون الاستئصال أكثر أو أقل شمولاً. وهكذا نميز:
استئصال بسيط للعقدة: تتم إزالة العقيدة فقط ، ويتم الحفاظ على باقي الغدة الدرقية ؛
استئصال الفص أو استئصال الفص: تتم إزالة فص واحد فقط من الغدة الدرقية. إنها الحالة الأكثر شيوعًا ؛
استئصال الغدة الدرقية “شبه الكلي”: لم يتبق سوى جزء من الغدة الدرقية في مكانه على كل جانب ؛
استئصال كامل للغدة الدرقية: استئصال الغدة الدرقية بالكامل ؛
استئصال الغدة الدرقية الكلي مع تشريح العقدة الليمفاوية ، وهو أكثر ندرة ، لبعض أنواع سرطان الغدة الدرقية.
اليوم ، تتمتع الفرق الطبية بأكثر المواقف تحفظًا.

علاج السرطان
في ايران
علاج السرطان الأكثر شيوعًا في إيران هو العلاج الكيميائي ، ولكن ...
علاج سرطان القولون
في ايران
عادةً ما تتضمن علاجات سرطان القولون والمستقيم عملية جراحية...
علاج سرطان المعدة
في ايران
أكثر أنواع علاج سرطان المعدة شيوعًا هي الجراحة والعلاج الكيميائي ...
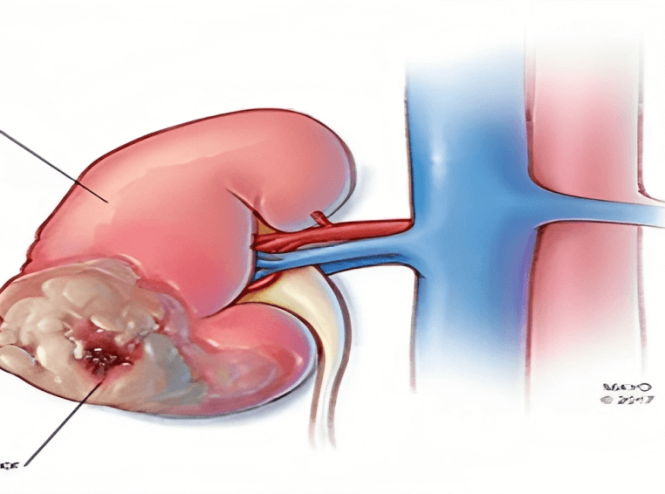
علاج سرطان الكلى في ايران
عادة ما يتم علاج سرطان الكلى بالجراحة والعلاج الموجه والعلاج المناعي ...
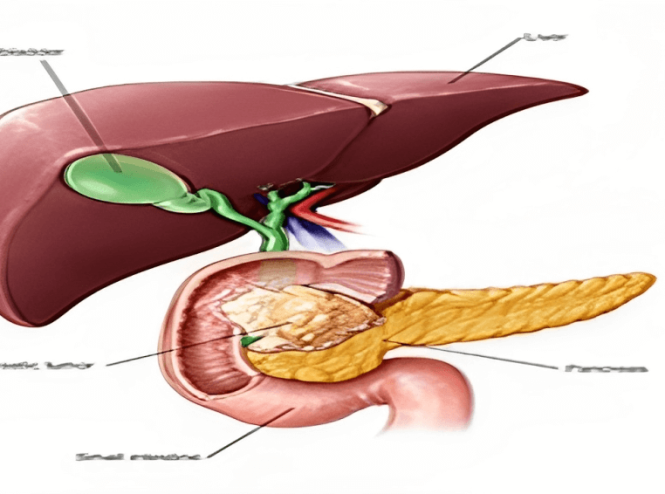
علاج سرطان البنكرياس في ايران
علاجات سرطان البنكرياس هي الجراحة أو العلاج الكيميائي أو مزيج منها
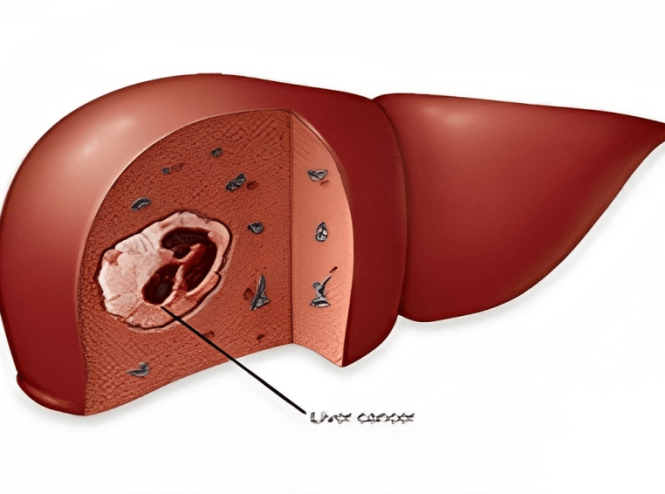
علاج سرطان الكبد
في ايران
أكثر علاجات سرطان الكبد فعالية هي الجراحة والعلاجات الموضعية
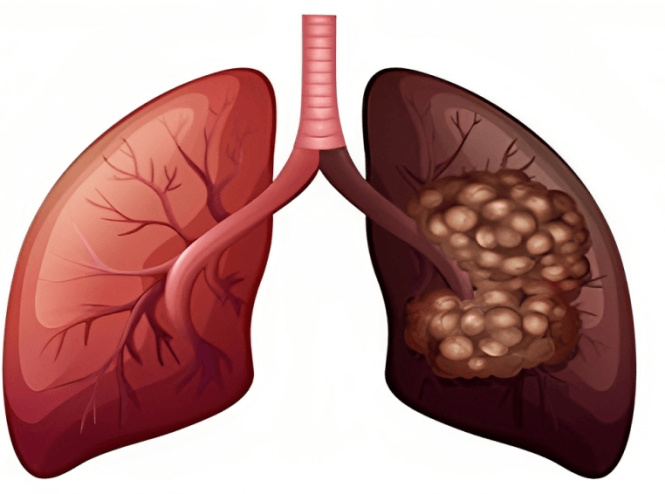
علاج سرطان الرئة في ايران
يمكن علاج سرطان الرئة بالجراحة والعلاج الكيميائي والعلاج الإشعاعي والعلاج الموجه ...
علاج سرطان المثانة في ايران
يُعالج سرطان المثانة عادةً بالجراحة أو العلاج الكيميائي أو الإشعاعي أو العلاج المناعي.
عقد عقد مع مراكز طبية صديقة للأطفال
- أول مركز زراعة قلب ناجح في إيران
- أول مركز زراعة نخاع عظمي في إيران
- أول مركز زراعة كلى في طهران
- أول مركز يقوم بإجراء الأشعة المقطعية في إيران
- أول مركز للتنظير الكبسولي بالفيديو في إيران
- مركز إحالة لعلاج أمراض الدم والأورام وعلاج سرطانات الدم بزراعة النخاع العظمي
- مركز مرموق لتدريب الزمالة في زراعة نخاع العظام وأمراض الدم والأورام في الدولة
- إنشاء بنك الخلايا الجذعية غير النسبي (مرتبط ببنك الخلايا الجذعية العالمي)
- القطب العلمي للطب النووي للبلاد
- مركز إحالة لعلاج السرطان بالأدوية الإشعاعية
- مركز التدريب الوحيد المعتمد من الوكالة الدولية للطاقة الذرية
- مركز جمعية الطب النووي الايراني
- مركز مجهز لعلاج أمراض الجهاز الهضمي والكبد
- المركز الوحيد الذي يقوم بإجراء تقنية POEM في علاج أمراض الجهاز الهضمي في الدولة
- مركز فائق التخصص لعلاج مشاكل الجهاز الهضمي ، بما في ذلك التشخيص والعلاج المتقدم ، بتقنية الجمع بين طريقتين تقنيتين ، “التنظير” و “التنظير التألقي”.
- من أرقى المراكز في العالم في مجال جراحة الوجه والفكين واستخدام الطابعات ثلاثية الأبعاد
- المركز الوحيد لعلاج جراحة الجنين بالليزر في الشرق الأوسط
- مركز مرموق في علاج عقم النساء وأطفال الأنابيب في الدولة
- المركز العلمي لعلاج أمراض الروماتيزم في الدولة
- خدمات تصوير الأوعية الدموية المتخصصة في علاج القدم السكرية
- خدمات التخصصات الدقيقة للعظام (استبدال مفصل الركبة ، جراحات تصحيح العمود الفقري للأطفال في الدولة)
دورة ما بعد الجراحة
دورة ما بعد الجراحة ليست مؤلمة للغاية ويمكن تخفيفها بسهولة عن طريق العلاج المسكن إذا لزم الأمر. يمكن استئناف الطعام في اليوم التالي للعملية. تتم إزالة النصف الأول من المواد الغذائية في اليوم التالي للعملية ، والنصف الآخر قبل التفريغ. تترك الندبة في الهواء الطلق بدون ضمادة ولا ينصح بتبليلها لمدة عشرة أيام.
يستمر الاستشفاء من 2 إلى 3 أيام
في حالة الاستئصال الكلي للغدة الدرقية ، فإن العلاج البديل بهرمونات الغدة الدرقية ضروري مدى الحياة. يبدأ أثناء العلاج في المستشفى ويوازنه الطبيب المعالج أو أخصائي الغدد الصماء. قد يكون هذا العلاج البديل ضروريًا أيضًا بعد الإزالة الجزئية إذا كان إفراز هرمونات الغدة الدرقية غير كافٍ.
اعتمادًا على مدى إزالة الغدة الدرقية ، والعلاج البديل المحتمل وطبيعة النشاط المهني ، يمكن أن يستمر التوقف عن العمل لمدة تصل إلى 3 أسابيع.
تقع الندبة في الطيات الطبيعية للرقبة ، لذا فهي عادة ما تكون غير مرئية بشكل كبير. لكن كل هذا يتوقف على جودة العلاج ، والتي تختلف من شخص لآخر.
استئصال الغدة الدرقية في ايران | أفضل مراكز ونتائج وتكلفة
المخاطر والمضاعفات
استئصال الغدة الدرقية هو إجراء بسيط مع مضاعفات نادرة جدا: ورم دموي ، نزيف ، عدم راحة في الجهاز التنفسي ، عدوى.
يمكن أن تظهر اضطرابات مختلفة ، غالبًا بشكل عابر:
صعوبة في البلع
بحة الصوت (تغيير في المسار) بسبب تلف الأعصاب المتكرر أثناء الإجراء والذي قد يتطلب ، في بعض الحالات ، علاج النطق ؛
تورم في منطقة العملية.
خلل في تنظيم الكالسيوم يمكن أن يسبب وخزًا وتشنجات ، بسبب تلف واحد أو أكثر من الغدد الجار درقية (الغدد المشاركة في تنظيم الكالسيوم) أثناء الإجراء. في بعض الأحيان تكون مكملات الكالسيوم وفيتامين د (ضرورية لإصلاح الكالسيوم) ضرورية. استئصال الغدة الدرقية هو نوع من التدخل الجراحي في الغدة الدرقية ، مما يعني إزالتها بالكامل مع تطور قصور الغدة الدرقية المستمر بعد الجراحة.
تتميز الغدة الدرقية بمجموعة متنوعة من الأمراض المختلفة الممرضة ، مثل الغروانية ، وتضخم الغدة الدرقية المتكاثر بدرجات متفاوتة ، والأورام الغدية ، والتهاب الغدة الدرقية المناعي الذاتي المزمن ، ومرض جريفز (تضخم الغدة الدرقية السام المنتشر) ، والأورام الخبيثة في الغدة الدرقية ، والتي تتطلب أساليب علاجية مختلفة ، في بعض الحالات ، قرار بشأن العلاج الجراحي.
تاريخ تطور جراحة الغدة الدرقية الحديثة لا يزيد عن 130-140 سنة. تمت مناقشة خطورة وتعقيد إجراء جراحة الغدة الدرقية من قبل الجراحين من جميع الأجيال. في وقت مبكر من عام 1928 ، كتب الجراح دي كيرفان “… أي شخص ، ليس لديه خلفية جراحية جيدة ، يخضع لإغراء إجراء عملية جراحية لنوع من تضخم الغدة الدرقية” الخفيف “، يجب ألا ينسى الحالات التي انتهت ، في أيدي عديمة الخبرة في الوفاة من فقدان الدم على طاولة العمليات “.
تطور العلاج الجراحي لأمراض الغدة الدرقية بسرعة في النصف الثاني من القرن التاسع عشر بسبب إدخال طرق التخدير العام. مؤسسو جراحة الغدة الدرقية هم الجراح النمساوي ألبرت ثيودور بيلروث والجراح السويسري إميل ثيودور كوشر.
كان ثيودور كوشير مؤيدًا نشطًا لاستئصال الغدة الدرقية الكلي في مرضى تضخم الغدة الدرقية. أتاحت مهارة Kocher في ذلك الوقت تقليل معدل الوفيات في مثل هذه العمليات من 38٪ إلى 0.3٪. بعد إجراء أول عملية جراحية في عام 1874 ، كانت عيادته حتى عام 1882 هي المركز الطبي الرئيسي في أوروبا للتدخلات الجراحية في الغدة الدرقية. كان تيودور كوشر هو الذي وصف في عام 1883 حالة الوذمة المخاطية التي تتطور بعد استئصال الغدة الدرقية ، والتي أطلق عليها اسم “Cachexia threopriva”. في عام 1909 ، حصل كوشر على جائزة نوبل في علم وظائف الأعضاء أو الطب تقديراً لإسهاماته الكبيرة في الفيزيولوجيا المرضية وجراحة الغدة الدرقية.
اقرأ المزيد: سرطان الثدي | علاج سرطان الثدي في ايران | جراحة الثدي مع أفضل جراح
في الوقت نفسه ، في عام 1883 ، نشر الجراح وعالم الطبيعة من جنيف ، جاك لويس ريفيردين ، مقالًا عن تطور الوذمة المخاطية بعد استئصال الغدة الدرقية بالكامل – “ميكسوديمي ما بعد الجراحة”. حتى تلك اللحظة ، لم يتم إثبات العلاقة بين الوذمة المخاطية ونتائج استئصال الغدة الدرقية. كان ريفيردين هو أول من اكتشف هذه الحقيقة وأثبتها ، لذلك يعتبر كل من كوشر وريفيردين مكتشفًا لقصور الغدة الدرقية بعد الجراحة.
بمرور الوقت ، تحسنت تقنية التدخل الجراحي في الغدة الدرقية. تم تطوير طرق مختلفة لمنع تطور مثل هذه المضاعفات الشديدة بعد الجراحة مثل شلل جزئي في الحنجرة مع اختلال وظيفي في الحنجرة وقصور الغدة الدرقية المستمر.
لسنوات عديدة ، كان اختيار مدى التدخل الجراحي في الغدة الدرقية إحدى المشكلات الرئيسية التي لم يتم حلها في جراحة الغدة الدرقية. في الوقت نفسه ، كان تعقيد التعويض الذي يحدث بعد الجراحة لقصور الغدة الدرقية هو العقبة الرئيسية أمام الإزالة الكاملة للغدة الدرقية. لفترة طويلة ، أدى الافتقار إلى الأدوية واستحالة دقة الجرعات في العلاج البديل إلى صعوبة تحقيق الغدة الدرقية المستقرة بعد الجراحة. كان هذا هو الدافع لاختيار الأساليب الجراحية التي تحافظ على الأعضاء عند إجراء عمليات الغدة الدرقية.
حتى منتصف القرن العشرين ، كان علاج قصور الغدة الدرقية ينطوي على إعطاء مستخلصات الغدة الدرقية للمرضى. لم تستطع هذه المستحضرات ، التي كان من المستحيل عمليا فيها إعطاء جرعة دقيقة من محتوى هرمونات الغدة الدرقية ، أن توفر بشكل كافٍ إفراز الغدة الدرقية المستقر ، وكان تناولها بحد ذاته مصحوبًا بصعوبات كبيرة. في عام 1913 ، قام عالم الكيمياء الحيوية الأمريكي الحائز على جائزة نوبل إدوارد كيلفن كيندال بعزل وتنقية هرمون الغدة الدرقية المتبلور وحقق زيادة قدرها 100 ضعف في تركيز الهرمونات في مستخلصات الغدة الدرقية ، والتي كانت بمثابة نقطة تحول في إنشاء مستحضرات هرمون الغدة الدرقية الحديثة. أدى إنشاء مستحضرات تركيبية بجرعات دقيقة من هرمونات الغدة الدرقية إلى تغيير جذري في فكرة علاج أمراض الغدة الدرقية وأدى إلى ثورة في أمراض الغدة الدرقية ، مما أدى إلى توسيع إمكانيات جراحة الغدة الدرقية.
في منطقتنا ، حتى عام 1995 ، للتعويض عن قصور الغدة الدرقية بعد الجراحة ، تم استخدام مستخلص الغدة الدرقية المجففة ، الغدة الدرقية ، والتي تمت معايرتها فقط بمحتوى اليود الكلي ، وتم تشكيل معظم العروض السريرية في فترة كانت هناك لا توجد مستحضرات حديثة من ليفوثيروكسين (L-T4). في هذا الصدد ، فيما يتعلق بأي مرض يصيب الغدة الدرقية ، كان هناك افتراض بأن قصور الغدة الدرقية هو أحد المضاعفات الشديدة لهذه الأمراض. أدى التوسع في إمكانية إجراء عمليات الغدة الدرقية إلى إلزام اختصاصيي الغدد الصماء بوضع مؤشرات صارمة للطرق الجراحية لعلاج أمراض الغدة الدرقية ، وذلك لتجنب النشاط التشغيلي المفرط.
المؤشرات المطلقة لاستئصال الغدة الدرقية هي جميع أشكال أورام الغدة الدرقية الخبيثة. بالنظر إلى حالة فترة ما بعد تشيرنوبيل وعواقب ما بعد الحادث ، يتم التعرف على استئصال الغدة الدرقية الكلي باعتباره الطريقة المفضلة حتى بالنسبة لسرطان الغدة الدرقية طفيف التوغل ، وسرطان الغدة الدرقية شديد التباين. يتيح التحقق الخلوي الإلزامي للتشخيص قبل الجراحة تحديد نطاق التدخل الجراحي المخطط له. فتح إجراء استئصال كامل للغدة الدرقية لسرطان الغدة الدرقية شديد التباين فرصًا للعلاج الفعال للنقائل باستخدام نظائر 131I وجعل من الممكن تحقيق نتائج علاجية مواتية.
في أغلب الأحيان ، يتم إجراء التدخلات الجراحية على الغدة الدرقية لتضخم الغدة الدرقية العقدي. وتجدر الإشارة إلى أن علم الغدة الدرقية الحديث لديه مجموعة واسعة من طرق التشخيص (الموجات فوق الصوتية ، والخلوية ، والهرمونية ، والإشعاعية) التي تتيح تحديد الأساس المرضي والمورفولوجي للمرض قبل العلاج ، وفي معظم الحالات ، تجنب التدخل الجراحي ، والاعتراف الحد الأدنى من مخاطر الأورام للتغيرات البؤرية المكتشفة في الغدة الدرقية. في معظم الحالات ، يتم تمثيل تضخم الغدة الدرقية العقدي عن طريق الغروية ، بدرجات متفاوتة ، تضخم الغدة الدرقية المتكاثر (حتى 90٪) ، والذي يخضع للمراقبة والعلاج المحافظ. عادةً ما تؤدي التدخلات الجراحية ذات الطبيعة التي تحافظ على الأعضاء في تضخم الغدة الدرقية المتكاثر العقيدات الغروانية إلى انتكاس المرض ، ويجب أن تكون هناك أسباب موضوعية جيدة لاستئصال الغدة الدرقية.
مؤشرات العلاج الجراحي للمرضى الذين يعانون من تضخم الغدة الدرقية العقدي هي:
السرطانات المؤكدة خلويًا.
الأورام المشبوهة ذات الطبيعة الخبيثة ؛
حالات التشخيص الخلوي المعقد (أورام الخلايا الجريبية والخلايا البائية – يصل تواتر الأورام الخبيثة في هذه المجموعة إلى 30٪) ؛
متلازمة الانضغاط الموضعي لأعضاء الرقبة ذات الأورام الحميدة الكبيرة ؛
الانسمام الدرقي مع تضخم الغدة الدرقية العقدي ومتعدد العقيدات كبير الحجم.
القضية الأكثر إثارة للجدل هي اختيار حجم التدخل الجراحي في مرض جريفز (تضخم الغدة الدرقية السام المنتشر). قبل توضيح التسبب في مرض جريفز ، كانت أيديولوجية العلاج الجراحي لهذا المرض على النحو التالي: في مريض مصاب بالتسمم الدرقي ، تم اكتشاف زيادة في حجم الغدة الدرقية في أغلب الأحيان ، ومن أجل تطبيع مستوى الغدة الدرقية. هرمونات الغدة الدرقية ، يجب إزالة جزء من العضو. كانت العملية الأكثر شيوعًا ولا تزال هي الاستئصال الجزئي للغدة الدرقية وفقًا لـ O.V. نيكولاييف. في وقت لاحق ، أصبح من الواضح أن مرض جريفز هو مرض مناعي ذاتي جهازي يتطور نتيجة إنتاج الأجسام المضادة لمستقبل الهرمون المنبه للغدة الدرقية (AT-rTSH) ، وترك جزء من الغدة الدرقية أثناء الاستئصال الجزئي. الهدف من تحفيز الأجسام المضادة في الجسم مما يؤدي إلى الانتكاس. الانسمام الدرقي. لذلك ، فإن النتيجة الوحيدة التي يمكن التنبؤ بها والهدف من العلاج الجراحي لمرض جريفز هو إزالة الغدة الدرقية بأكملها. في هذا الصدد ، وفقًا للمفاهيم الحديثة في الآونة الأخيرة ، لم يعد يُعتبر قصور الغدة الدرقية أحد مضاعفات التدخل الجراحي في مرض جريفز وأصبح في الواقع هدف العلاج.
وفقًا لأدبيات السنوات الأخيرة ، فإن الاستئصال الجزئي للغدة الدرقية لمرض جريفز هو منطقيًا (يعتمد على التسبب في المرض) وغير مبرر عمليًا. في معظم العيادات الأجنبية ، أصبحت العملية المفضلة لمرض جريفز ، “المعيار الذهبي” ، هي استئصال الغدة الدرقية.
في العقد الماضي ، ظهر عدد كبير من الأعمال المكرسة لمشكلة قصور الغدة الدرقية ، والتي غيرت وجهات نظرنا حول أمراض الغدة الدرقية. بادئ ذي بدء ، يرجع هذا إلى إدخال مستحضرات هرمون الغدة الدرقية الحديثة في الممارسة السريرية. على خلفية تناول هذه الأدوية ، يصبح قصور الغدة الدرقية بالنسبة للمريض ليس مرضًا ، ولكنه أسلوب حياة لا ينطوي عمليًا على أي قيود خاصة. لا تختلف المستحضرات الاصطناعية الحديثة ذات الجرعات الدقيقة من الليفوثيروكسين (L-T4) في التركيب عن هرمون الغدة الدرقية البشري (T4) وتجعل من الممكن بسهولة وفعالية الحفاظ على حالة الغدة الدرقية المستقرة على خلفية تناولها مرة واحدة فقط في اليوم.
المتطلبات الأساسية لذلك هي عوامل مثل:
الوظيفة الحيوية الوحيدة للغدة الدرقية هي إنتاج هرمونات الغدة الدرقية.
الإيقاع اليومي لإفراز هرمونات الغدة الدرقية غائب عمليًا (الاختلاف من يوم لآخر أقل من 15 ٪) ، وبالتالي ، فإن الاستهلاك اليومي من الليفوثيروكسين (L-T4) في نفس الجرعة يصوغ بسهولة إنتاجها الداخلي ؛
استقرار حاجة الجسم لهرمونات الغدة الدرقية (الحالات النادرة التي تتطلب تغيير الجرعة المختارة من L-T4 هي تغييرات واضحة في وزن الجسم والحمل والإعطاء الموازي لبعض الأدوية) ؛
التوافر البيولوجي العالي لـ L-T4 عند تناوله عن طريق الفم ؛
عمر النصف الطويل للبلازما من L-T4 (حوالي 7 أيام) ؛
وجود معيار دقيق (مستوى TSH) ، والذي يعكس تمامًا جودة تعويض قصور الغدة الدرقية لفترة طويلة (حوالي 2-3 أشهر) ؛
الرخص النسبي لمستحضرات L-T4 ؛
لا تختلف جودة حياة المرضى الذين يعانون من قصور الغدة الدرقية والذين يتلقون باستمرار العلاج البديل L-T4 عمليًا بشكل كبير عن أولئك الذين لا يعانون من قصور الغدة الدرقية.
الهدف من العلاج البديل لقصور الغدة الدرقية هو الحفاظ على مستوى ثابت من هرمونات الغدة الدرقية في الجسم التي تلبي الاحتياجات الفسيولوجية. المؤشر الرئيسي لتقييم مدى كفاية العلاج البديل لقصور الغدة الدرقية هو مستوى الهرمون المحفز للدرقية ، الذي تحدده طرق ذات حساسية وظيفية عالية.
مبادئ العلاج البديل لقصور الغدة الدرقية معروفة جيدًا. تلخص الإرشادات الدولية للتشخيص المختبري لأمراض الغدة الدرقية هذه الأعراض بإيجاز شديد:
تُفضل مستحضرات ليفوثيروكسين (L-T4) للعلاج ببدائل قصور الغدة الدرقية.
عادة ما يتم تحقيق إفراز الغدة الدرقية عند البالغين عن طريق إعطاء L-T4 بجرعة 1.6 ميكروغرام / كجم من وزن الجسم يوميًا. الحاجة إلى L-T4 عند الأطفال أعلى بكثير ويمكن أن تصل إلى 4 ميكروغرام / كغ في اليوم. يتم تحديد الجرعة الأولية من الدواء ووقت الوصول إلى جرعة الاستبدال الكاملة بشكل فردي ، اعتمادًا على العمر ووزن الجسم ووجود أمراض القلب المصاحبة.
تقل الحاجة إلى L-T4 مع تقدم العمر. قد يتلقى بعض كبار السن أقل من 1 ميكروغرام / كجم من L-T4 يوميًا.
تزداد الحاجة إلى L-T4 أثناء الحمل. يُنصح بتقييم وظيفة الغدة الدرقية عند النساء الحوامل ، والذي يتضمن دراسة مستوى TSH و T4 المجاني ، في كل ثلاثة أشهر من الحمل. يجب أن تكون جرعة L-T4 كافية للحفاظ على مستويات TSH الطبيعية ومستويات T4 المجانية.
في النساء اللواتي يعانين من قصور الغدة الدرقية بعد سن اليأس على العلاج ببدائل الاستروجين ، قد تكون الزيادة في جرعة L-T4 ضرورية للحفاظ على مستويات TSH الطبيعية.
الهدف من العلاج البديل لقصور الغدة الدرقية الأولي هو الحفاظ على مستوى TSH في حدود 0.5 – 1.5 ملي / لتر.
تتغير مستويات TSH ببطء بعد تغيير جرعة L-T4 أو وصف دواء مختلف ؛ يتم فحصه في موعد لا يتجاوز 6-8 أسابيع بعد تعيين جرعة بديلة كاملة.
لتقييم مدى كفاية جرعة L-T4 ، بعد 2-3 أشهر من تعيين جرعة بديلة كاملة ، من الضروري تحديد مستوى TSH. إذا ظل مستوى TSH مرتفعًا ، فيجب زيادة جرعة L-T4 بمقدار 25 ميكروغرام ، متبوعة بمراقبة TSH بعد 6-8 أسابيع.
يُنصح المرضى الذين يتلقون جرعة معايرة من L-T4 بفحص مستويات TSH سنويًا. لا يتأثر مستوى TSH بوقت أخذ عينات الدم والفاصل الزمني بعد أخذ L-T4. بالإضافة إلى ذلك ، إذا تم استخدام تحديد مستوى T4 المجاني لتقييم مدى كفاية العلاج ، فلا ينبغي تناول الدواء في الصباح قبل أخذ عينات الدم ، لأنه لمدة 9 ساعات تقريبًا بعد أخذ L-T4 ، فإن المستوى تزداد نسبة T4 في الدم بشكل ملحوظ (بنسبة 15 – 20٪).
من الناحية المثالية ، يجب تناول L-T4 على معدة فارغة قبل 30 إلى 40 دقيقة من الوجبات ، في نفس الوقت من اليوم ، وعلى الأقل 4 ساعات قبل أو بعد الأدوية أو الفيتامينات الأخرى.
قد يتطلب تناول الأدوية والمركبات مثل الكوليسترول ، والكبريتات الحديدية ، وبروتينات الصويا ، والسكرالفات ، ومضادات الحموضة التي تحتوي على هيدروكسيد الألومنيوم ، والتي تقلل من امتصاص L-T4 ، زيادة جرعتها.
اليوم ، المستحضرات الاصطناعية الأكثر انتشارًا من ليفوثيروكسين – شركة Nycomed “Eutiroks”. أثبت الدواء نفسه في الاستخدام العملي ، وهو سهل الجرعات ، وبالجرعة الصحيحة لا يسبب آثارًا جانبية.
بعد العلاج الجذري لسرطان الغدة الدرقية شديد التباين ، يجب أن يخضع المرضى للعلاج القمعي باستخدام مستحضرات هرمون الغدة الدرقية التي تهدف إلى تصحيح قصور الغدة الدرقية بعد الجراحة وقمع النمو المعتمد على TSH لخلايا الورم المتبقية. الدواء المختار هو ليفوثيروكسين (L-T4) ؛ استخدام ثلاثي يودوثيرونين (liothyronine L-T3) غير مقبول للعلاج طويل الأمد ويقتصر على الدورات القصيرة لإعداد المريض للتصوير الومضاني باستخدام 131I. بالنسبة لمعظم المرضى ، يتم عرض تحقيق قمع مستوى TSH إلى الحد الأدنى من الأرقام التي يمكن اكتشافها في النطاق من 0 – 0.05 mU / l. يتم التحكم في مستويات TSH بعد 3 أشهر على الأقل من العلاج الأولي. يتم تعديل جرعة L-T4 بشكل أكبر عن طريق إنقاصها أو زيادتها بمقدار 25 ميكروغرام / يوم مع المراقبة المتكررة لـ TSH في المصل بعد 3 أشهر. عندما يتم الوصول إلى الجرعة المثلى من L-T4 ، ليست هناك حاجة للتحكم في مستوى T4 و T3 المجاني في مصل الدم ، ويتم مراقبة مستوى TSH كل 6-12 شهرًا. في المرضى الذين يعانون من مغفرة غير مؤكدة للمرض أثناء العلاج ، يوصى بالعلاج القمعي لمدة 3-5 سنوات.
غالبًا ما تتجلى الآثار الجانبية في شكل التسمم الدرقي تحت الإكلينيكي من خلال أعراض القلب وهشاشة العظام. أظهرت الدراسات بأثر رجعي أن هذه التأثيرات تكون ضئيلة عند اختيار جرعة مناسبة من L-T4 ومراقبتها بعناية لتجنب مستويات الدم الزائدة من T4 و T3 المجاني. ومع ذلك ، في المرضى المسنين أو في المرضى الذين يعانون من أمراض القلب التي تؤدي إلى تفاقم حالة المريض ، من الممكن الامتناع عن إجراء العلاج القمعي. يجب أن يؤخذ في الاعتبار أنه أثناء التسمم الدرقي تحت الإكلينيكي ، يكون ملف تعريف البروثرومبين مضطربًا في معظم المرضى.
من المهم أيضًا التحكم في استقلاب الكالسيوم في المرضى الذين خضعوا لعملية استئصال الغدة الدرقية. في بعض الحالات ، يجب تعويض قصور الغدة الجار درقية العابر الذي يحدث في أول 6-12 شهرًا بعد الجراحة عن طريق تناول مكملات الكالسيوم (كالسيوم D3 نيكوميد) بالاشتراك مع الشكل النشط لفيتامين د (تاهيستين ، α – D 3) في اختيار فردي جرعات.